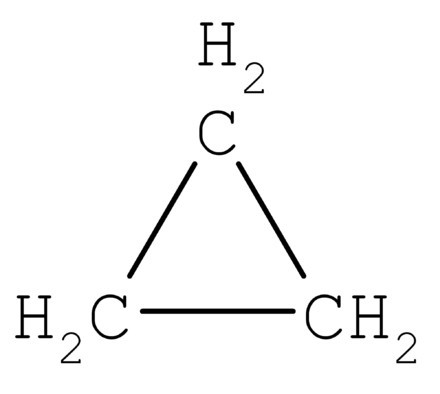
Alifatische koolwaterstoffen zijn wat?
Alifatische koolwaterstoffen zijn organische verbindingen waarvan de moleculen slechts één enkele binding bevatten. Deze omvatten alkanen en cycloparaffinen, hun eigenschappen zullen in ons materiaal worden beschouwd.

De algemene formule van alkanen
Vertegenwoordigers van deze klasse worden gekenmerkt doordoor de algemene formule CnH2n + 2. Paraffines omvatten alle verbindingen met een open keten, waarbij de atomen worden samengevoegd door eenvoudige bindingen. Vanwege het feit dat onder normale omstandigheden alifatische koolwaterstoffen laagactieve verbindingen zijn, hebben ze hun naam "paraffines" gekregen. We zullen enkele kenmerken van de structuur van vertegenwoordigers van deze klasse verduidelijken, de aard van de binding in moleculen, het toepassingsgebied.

Korte beschrijving van methaan
Als de eenvoudigste vertegenwoordiger van deze klasse kunnen we methaan noemen. Hij is het die de alifatische reeks koolwaterstoffen begint. We onthullen de onderscheidende kenmerken ervan.
Methaan is onder normale omstandighedeneen gasachtige substantie die geurloos en kleurloos is. Deze verbinding wordt in de natuur gevormd door ontleding zonder de aanwezigheid van luchtzuurstof van dieren en plantenorganismen. Het wordt bijvoorbeeld aangetroffen in aardgas en wordt daarom momenteel in grote hoeveelheden gebruikt als brandstof in de productie en in het dagelijks leven.
Wat voor soort chemische binding hebben deze koolwaterstoffen? Alifatische, beperkende organische verbindingen zijn covalente polaire moleculen.
Het methaanmolecuul heeft een tetraëdrische vormmolecuul, het type hybridisatie van koolstofatomen daarin sp3, wat overeenkomt met een valentiehoek van 109 graden 28 minuten. Het is om deze reden dat alifatische koolwaterstoffen chemisch laagactieve verbindingen zijn.

Kenmerken van methaan-homologen
Naast methaan in aardgas en olie,Andere koolwaterstoffen, die er een vergelijkbare structuur mee hebben. De eerste vier vertegenwoordigers van de homologe reeks paraffinen bevinden zich in de gasvormige aggregaattoestand, hebben een onbetekenende oplosbaarheid in water.
Als de relatieveDe toename van de kook- en smeltpunten van CdHy wordt waargenomen in de molecuulmassa. Tussen de individuele vertegenwoordigers van de serie is er een duidelijk verschil CH2, dat het homologische verschil wordt genoemd. Het is een directe bevestiging van de aansluiting van de compound op deze organische serie.
Alle alifatische koolwaterstoffen zijn stoffen die gemakkelijk oplosbaar zijn in organische oplosmiddelen.

Isomerie van series
Voor vertegenwoordigers van een aantal paraffines is kenmerkendisomerie van het koolstofskelet. Dit wordt verklaard door de mogelijkheid van ruimtelijke rotatie van het koolstofatoom rond chemische bindingen. Om bijvoorbeeld de samenstelling van C4H10 aan te sluiten, kunt u een koolwaterstof met een recht koolstofskelet - butaan gebruiken. Omdat de structurele isomeer 2-methylpropaan is, dat een vertakte structuur heeft.
Onder typische chemische eigenschappen, kenmerkendvoor paraffines is het noodzakelijk om de substitutiereacties te noteren. De verzadiging van de bindingen verklaart de complexiteit van de reactie, het radicale mechanisme ervan. Om gehalogeneerde derivaten van alifatische koolwaterstoffen te verkrijgen, is het noodzakelijk om de halogeneringsreactie uit te voeren in aanwezigheid van UV-straling. Het ketenkarakter van deze interactie wordt waargenomen in alle vertegenwoordigers van deze serie. De resulterende producten worden halogeenderivaten genoemd. Ze worden veel gebruikt in de chemische industrie als organische oplosmiddelen.
Bovendien zijn alle alifatische en aromatischekoolwaterstoffen verbranden in aanwezigheid van zuurstof en vormen water en koolstofdioxide. Afhankelijk van het percentage gehalte in het koolstofmolecuul, wordt een andere hoeveelheid warmte afgegeven. Ongeacht of ze tot de klasse van organische verbindingen behoren, alle verbrandingsprocessen zijn exotherme reacties die in het dagelijks leven en in de industrie worden gebruikt.
Dehydrogenatie van methaan (waterstofsplitsing) heeft ook praktische toepassing. Als gevolg van dit proces wordt acetyleen gevormd, wat een waardevolle chemische grondstof is.

Het gebruik van alkanen en gechloreerde alkanen
Dichloormethaan, chloroform, tetrachloorethaan - vloeistoffen,die uitstekende organische oplosmiddelen zijn. Chloroform en jodoform worden gebruikt in de moderne geneeskunde. De afbraak van methaan is een van de industriële methoden voor de productie van roet, wat nodig is voor de productie van drukinkt. Methaan wordt beschouwd als de belangrijkste bron van de productie van gasvormig waterstof in de chemische industrie, die gaat naar de productie van ammoniak, en ook naar de synthese van talrijke organische stoffen.
Onverzadigde koolwaterstoffen
Onverzadigde alifatische koolwaterstoffen zijnvertegenwoordigers van een aantal ethyleen en acetyleen. Laten we hun basiseigenschappen en toepassingen analyseren. De alkenen worden gekenmerkt door de aanwezigheid van een dubbele binding, dus de algemene formule voor de reeks heeft de vorm CnH2n.
Gezien de onverzadigde aard van deze stoffen,er kan worden opgemerkt dat ze de reactie van de verbinding aangaan: hydrogenering, halogenering, hydratatie, hydrohalogenering. Bovendien zijn vertegenwoordigers van een aantal ethyleen in staat tot polymerisatie. Het is dit specifieke kenmerk dat vertegenwoordigers van deze klasse veel gevraagd maakt in de moderne chemische productie. Polyethyleen en polypropyleen zijn de stoffen die de basis vormen van de polymeerindustrie.
Acetyleen is de eerste vertegenwoordiger van een serieDe algemene formule is CnH2n-2. Onder de onderscheidende kenmerken van deze verbindingen kan men de aanwezigheid van een drievoudige binding onderscheiden. De aanwezigheid ervan verklaart het verloop van de reacties van de verbinding met halogenen, water, waterstofhalogenide, waterstof. Als de drievoudige binding in dergelijke verbindingen zich in de eerste positie bevindt, dan is voor alkynen een kwalitatieve substitutiereactie met een complex zilverzout kenmerkend. Het is dit vermogen dat een kwalitatieve reactie is op een alkyn, gebruikt om het te detecteren in een mengsel met een alkeen en een alkaan.
Aromatische koolwaterstoffen zijn cyclische onverzadigde verbindingen, daarom worden ze niet beschouwd als alifatische verbindingen.

conclusie
Ondanks de verschillen in de kwantitatieve samenstelling,bestaande in vertegenwoordigers van beperkende en onverzadigde alifatische verbindingen, ze zijn qua kwaliteit vergelijkbaar, bevatten koolstof en waterstof in de moleculen. Verschillen in de kwantitatieve samenstelling (verschillende algemene formules) in de vertegenwoordigers van verzadigde en onverzadigde CC12 verklaren het verschil in de mechanismen van de reacties om verschillende producten te verkrijgen.
Dat is de reden waarom vertegenwoordigers van alle klassen van dergelijkeverbindingen gaan verbrandingsreacties in, vormen koolstofdioxide, water en geven een bepaalde hoeveelheid thermische energie af, waardoor ze als brandstof in het dagelijks leven en in de industrie van pas komen.
</ p>